Dermatite esfoliativa in un bambino con sindrome di Omenn
03/10/2020
Immunodeficienza da deficit di Artemis
(Ultimo aggiornamento: 03/10/2020)
Il gene DNA cross-link repair 1C (DCLRE1C) (OMIM *605988), codifica per la proteina Artemis, il cui nome evoca quello di una divinità greca associata con la fertilità. DCLRE1C è indispensabile per la ricombinazione dei geni variabili V(D)J dei recettori TCR e BCR espressi rispettivamente sui linfociti T e B e per lo svolgimento della NHEJ che permette la riparazione dei danni subiti dalla doppia elica del DNA (Vedere "SCID T-B-NK+ Eziopatogenesi ed epidemiologia "). Durante la NHEJ, Artemis sembra interagire in modo preferenziale con DNA-PK [1, 2], il cui deficit è anch’esso causa di SCID T-B-NK+. La ricombinazione V(D)J è uno dei meccanismi che assicurano l’enorme amplificazione e diversificazione delle specificità antigeniche riconosciute dai suddetti recettori che, globalmente arrivano a riconoscere oltre 1012-1014 antigeni diversi. Per la sua importanza nel mantenimento della stabilità della sequenza del DNA DCLRE1C è considerato uno dei custodi del genoma [3], DCLRE1C mappa sul cromosoma 10p13 e contiene 14 esoni [4]. La proteina Artemis consta di 685 aminoacidi, ha una massa molecolare di 77,6 kD e ha un’omologia di struttura del 78% con l’equivalente proteina murina [4].
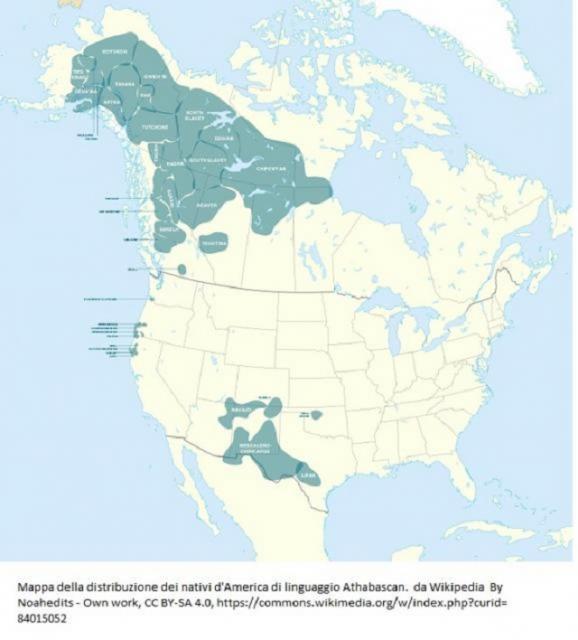
Il fenotipo clinico del deficit di Artemis varia da quello di una SCID T-B-NK+ con aumentata sensibilità alle radiazioni ionizzanti a quello di una SCID leaky o attenuata che può essere indistinguibile alla sindrome di Omenn da deficit di RAG1/RAG2 [5, 6].(Vedere " SCID T-B-NK+ Manifestazioni cliniche, diagnosi e terapia") Il deficit di Artemis è una delle cause più rare di immunodeficienza primitiva , essendogli attribuiti poco più dell’un percento dei casi di SCID T-B-NK+[7]. La frequenza relativa del deficit di Artemis è più elevata nelle popolazioni native degli Indiani d’America di linguaggio Athabascan [8].
La diagnosi e la terapia non sono dissimili da quanto già descritto per le altre SCID. (Vedere "SCID- Cenni di terapia medica ") Il trapianto di midollo può guarire il deficit di Artemis, anche se è preferibile usare protocolli di condizionamento a dose ridotta per evitare eccessiva tossicità conseguente all’aumentata sensibilità agli effetti collaterali delle radiazioni e dei farmaci citotossici [9].
Riferimenti bibliografici
- Ma Y, Pannicke U, Schwarz K, Lieber MR: Hairpin opening and overhang processing by an Artemis/DNA-dependent protein kinase complex in nonhomologous end joining and V(D)J recombination. Cell 2002, 108(6):781-794. https://www.ncbi.nlm.nih.gov/pubmed/11955432.
- Malu S, De Ioannes P, Kozlov M, Greene M, Francis D, Hanna M, Pena J, Escalante CR, Kurosawa A, Erdjument-Bromage H et al: Artemis C-terminal region facilitates V(D)J recombination through its interactions with DNA Ligase IV and DNA-PKcs. J Exp Med 2012, 209(5):955-963. https://www.ncbi.nlm.nih.gov/pubmed/22529269.
- Kinzler KW, Vogelstein B: Cancer-susceptibility genes. Gatekeepers and caretakers. Nature 1997, 386(6627):761, 763. https://www.ncbi.nlm.nih.gov/pubmed/9126728.
- Moshous D, Callebaut I, de Chasseval R, Corneo B, Cavazzana-Calvo M, Le Deist F, Tezcan I, Sanal O, Bertrand Y, Philippe N et al: Artemis, a novel DNA double-strand break repair/V(D)J recombination protein, is mutated in human severe combined immune deficiency. Cell 2001, 105(2):177-186. https://www.ncbi.nlm.nih.gov/pubmed/11336668.
- Le Deist F, Moshous D, Villa A, Al-Herz W, Roifman CM, Fischer A, Notarangelo LD: Combined T- and B-Cell Immunodeficiencies. In: Primary Immunodeficiency Diseases: Definition, Diagnosis, and Management. edn. Edited by Rezaei N, Aghamohammadi A, Notarangelo LD. Berlin, Heidelberg: Springer; 2017: 83-182.
- Ege M, Ma Y, Manfras B, Kalwak K, Lu H, Lieber MR, Schwarz K, Pannicke U: Omenn syndrome due to ARTEMIS mutations. Blood 2005, 105(11):4179-4186. https://www.ncbi.nlm.nih.gov/pubmed/15731174.
- Buckley RH: Molecular defects in human severe combined immunodeficiency and approaches to immune reconstitution. Annu Rev Immunol 2004, 22:625-655. https://www.ncbi.nlm.nih.gov/pubmed/15032591.
- Li L, Moshous D, Zhou Y, Wang J, Xie G, Salido E, Hu D, de Villartay JP, Cowan MJ: A founder mutation in Artemis, an SNM1-like protein, causes SCID in Athabascan-speaking Native Americans. J Immunol 2002, 168(12):6323-6329. https://www.ncbi.nlm.nih.gov/pubmed/12055248.
- Roifman CM: 35 - Primary T-Cell Immunodeficiencies. In: Clinical Immunology (Fifth Edition). edn. Edited by Rich RR, Fleisher TA, Shearer WT, Schroeder HW, Frew AJ, Weyand CM. London: Content Repository Only!; 2019: 489-508.e481.
