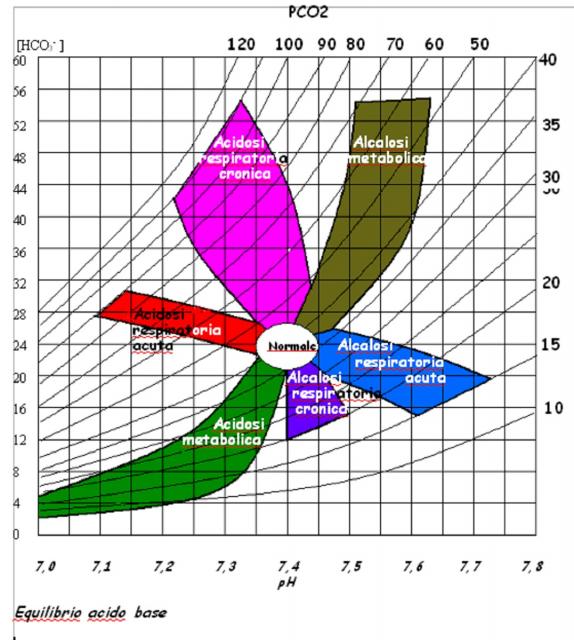
Equilibrio acido base, nomogramma da WIkipedia
04/04/2020
Definizioni, fisiologia e valutazione dello stato acido-base con l’ emogasanalisi arteriosa
(Ultimo aggiornamento: 15/11/2020)
L’equilibrio acido-base e i suoi disordini si valutano misurando la quantità di ognuno dei componenti il sistema tampone bicarbonato-carbonio nel sangue: anidride carbonica, idrogeninioni e bicarbonati. In condizioni fisiologiche vi è un equlibrio fra queste tre componenti secondo l’equazione:
CO2 disciolto + H2O ↔ H2CO3 ↔ HCO3- + H+
Di questi, la pressione parziale della CO2 (PCO2) e il pH vengono misurati direttamente mediante elettrodi analitici, mentre la concentrazione del bicarbonato (HCO3-) viene calcolata con l'equazione di Henderson-Hasselbalch, nella quale la PCO2 è espressa in mmHg e HCO3- in mEq/L:
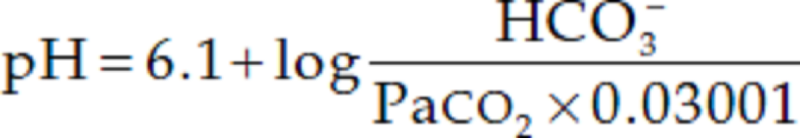
dove il pH è uguale al logaritmo negativo della concentrazione degli idrogenioni [H+]; 6.10 è il log negativo di Ka (-log Ka), che è la costante di dissociazione per questa reazione; PCO2 è la pressione parziale dell'anidride carbonica nel sangue e 0,03001 è il suo coefficiente di solubilità nel sangue;
I bicarbonati nel sangue venoso, di solito vengono misurati direttamente come "CO2 totale" con un elettrodo selettivo per gli ioni. La "CO2 totale" misurata direttamente è generalmente di circa 2 mEq/L maggiore dell' HCO3 calcolato contemporaneamente nel sangue arterioso.
Valori normali nel sangue venoso e arterioso
L’intervallo dei i valori normali dei vari parametri necessari per valutare l’equilibrio acido-base è diverso nel sangue arterioso rispetto a quello venoso e varia notevolmente anche fra i diversi laboratori.
Sangue arterioso
Nel sangue arterioso, l'intervallo normale del pH è compreso tra 7,35 e 7,45; la concentrazione del bicarbonato (HCO3-) tra 21 a 27 mEq/L mentre la concentrazione della PCO2, varia 35 a 45 mmHg.
Sangue venoso periferico
I valori normali nel sangue venoso periferico sono diversi da quelli del sangue arterioso a causa dell'assorbimento e del tamponamento della CO2 prodotta metabolicamente nella circolazione capillare e dell'aggiunta degli acidi organici prodotti e drenati nel circolo venoso. Diversi studi hanno evidenziato che il pH venoso periferico è di circa 0,03- 0,04 unità inferiore rispetto al sangue arterioso; la concentrazione di HCO3 è di circa 1-2 mEq/L superiore, e la PCO2 è di circa 3-8 mmHg superiore [1–3]. Se per il monitoraggio seriale viene utilizzato il sangue venoso, deve essere eseguito periodicamente un controllo con il sangue arterioso [2,4,4].
Sangue venoso centrale
In pazienti con cateteri venosi centrali si possono usare i campioni venosi centrali. Il pH venoso centrale è di solito da 0,03 a 0,05 unità di pH inferiore rispetto al sangue arterioso e la PCO2 e di circa 5 mmHg più alta, mentre le concentrazioni di HCO3- sono sostanzialmente equivalenti a quelle del sangue venoso periferico o arterioso [4,5].
Definizioni dei disordini acido-base
Sulla base dei principi dell'equazione di Henderson-Hasselbalch, le definizioni quasi universalmente accettate per la definizione dei disordini del metabolismo acido-base sono le seguenti:
Acidemia – Un pH arterioso al di sotto del valore normale (< 7,35).
Alcalemia – Un pH arterioso al di sopra del valore normale (> 7,45).
Acidosi – Un processo che tende ad abbassare il pH dei liquidi extracellulari e quindi del sangue (aumenta la concentrazione di ioni di idrogeno). La riduzione del pH è causata primariamente da una diminuta concentrazione di bicarbonato nel siero (HCO3) e/o da un aumento della PCO2.
Alcalosi – Un processo che tende ad aumentare il pH del fluido extracellulare e del sangue (la concentrazione di ioni di idrogeno diminuisce). Tale aumento può osservarsi per aumento della concentrazione di HCO3 nel sangue e/o da una diminuzione della PCO2.
Acidosi metabolica – Un disturbo che riduce la concentrazione di HCO3 nel siero e il pH ematico.
Alcalosi metabolica – Un disturbo che aumenta la concentrazione di HCO3 nel siero e il pH ematico.
Acidosi respiratoria – Un disturbo che aumenta la PCO2 arteriosa e riduce il pH.
Alcalosi respiratoria – una condizione che riduce la PCO2 e aumenta il pH.
(vedere anche "Introduzione ai disturbi dell'equilibrio acido-base")
Disturbi dell’equilibrio acido base semplici e misti
Per disturbo semplice dell’equilibrio acido-base si intende la presenza di una delle suddette condizioni associata alla prevista adeguata risposta compensatoria respiratoria o renale per quello stesso disturbo.
I disturbi misti dell’equilibrio acido- base sono definiti come disturbi che coesistono nello stesso paziente in modo indipendente e non sono semplicemente una risposta compensatoria ad un’alterazione primaria [6]. Per una corretta diagnosi dei disturbi misti dell’equilibrio acido-base è necessario anche: calcolare il gap anionico (anion gap, AG), o divario degli anioni; conoscere il valore dell’albuminemia per effettuare la correzione per un normale valore di albumina sierica di 4,5 g/dL; stabilire se una risposta respiratoria o renale compensatoria sia minore o superiore rispetto all’atteso. La storia del paziente può fornire indizi importanti per una corretta diagnosi. Un paziente con chetoacidosi diabetica (acidosi metabolica) può sviluppare una malattia respiratoria indipendente (ad esempio, una polmonite) che potrebbe causare un'acidosi o alcalosi respiratoria sovrapposta. I pazienti con malattia polmonare sottostante (ad esempio, broncopneumopatia cronica ostruttiva) potrebbero non rispondere all'acidosi metabolica con un'adeguata risposta ventilatoria a causa di una riserva respiratoria insufficiente. Un paziente con vomito grave dovrebbe sviluppare un'alcalosi metabolica a causa della perdita di liquido gastrico acido. Se, tuttavia, il paziente sviluppasse anche shock ipovolemico a seguito della perdita di liquidi, l'acidosi lattica potrebbe abbassare il bicarbonato precedentemente elevato riportandolo a valori “normali”, con conseguente acidemia. Il sovrapporsi di un’acidosi respiratoria sull'acidosi metabolica può portare a una grave acidemia. Quando l'acidosi metabolica e l'alcalosi metabolica coesistono nello stesso paziente, il pH può essere normale. In casi del genere, è solo la presenza di un AG elevato (vedi sotto) che suggerisce la presenza di un'acidosi metabolica.
La terminologia comunemente utilizzata per analizzare i parametri di laboratorio necessari per la diagnosi dei disturbi dell'equilibrio acido-base può essere fonte di confusione. Soprattutto quando si parla di PCO2, bicarbonati totali, CO2 totale, bicarbonati standard ed eccessi di base [7]. Pertanto, può essere utile conoscere il reale significato di questi termini e come questi parametri di laboratorio sono acquisiti. La maggioranza dei laboratori effettua l’emogasanalisi mediante analizzatori dedicati alla misurazione dei gas, e questi solitamente misurano direttamente soltanto due dei parametri forniti con l'emogasanalisi: la concentrazione arteriosa degli idrogenioni e la concentrazione della CO2 o PaCO2. I bicarbonati e il pH sono calcolati con apposite formule [7].
Molti laboratori misurano la concentrazione della CO2 totale nel profilo elettrolitico standard. Il motivo di questa scelta è che risulta tecnicamente difficile misurare direttamente la concentrazione degli ioni bicarbonato nella soluzione, mentre è relativamente più agevole misurare la CO2 totale. La CO2 totale risulta dalla quantità totale di ioni bicarbonato sommata alla CO2 disciolta e a quella legata ad altre sostanze presenti nella soluzione. Dal momento che il bicarbonato costituisce la maggioranza della CO2 totale, questa viene spesso utilizzata come un surrogato affidabile della concentrazione dei bicarbonati. Anche se la CO2 totale può fornire una spia della presenza di un disturbo acido-base, la diagnosi definitiva non può basarsi sulla sola quantità di CO2 presente nel campione.
I bicarbonati standard sono considerati un indice che dovrebbe fornire informazioni sulla concentrazione attesa o teorica di bicarbonati, qualora fosse possibile eliminare la componente respiratoria dai disordini metabolici. Il cosiddetto eccesso di basi è un altro indice calcolato che può aumentare nell'alcalosi metabolica e diminuire nell'acidosi metabolica.
Una ridotta concentrazione di bicarbonato significa generalmente che il più importante dei sistemi tampone dell'organismo viene utilizzato per neutralizzare l'eccesso di acido (idrogenioni) che si produce, per esempio, nella chetoacidosi o nell'acidosi lattica. Un'altra spiegazione può essere che la concentrazione dei bicarbonati è ridotta a causa di perdite attraverso il tratto gastrointestinale (diarrea) o nei pazienti con malattie renali, nei quali possono essere ridotti sia la sintesi di nuovi bicarbonati che il riassorbimento tubulare di quelli filtrati con conseguente perdita nelle urine. La riduzione della concentrazione dei bicarbonati è la caratteristica distintiva dell'acidosi metabolica.
Un aumento della concentrazione dei bicarbonati indica che vi sono state perdite significative di acidi dai fluidi corporei, per esempio in seguito a prolungata aspirazione nasogastrica o vomito persistente. L'aumento dei bicarbonati può esprimere anche il compenso cronico da parte dei reni in soggetti con ipoventilazione da malattie respiratorie croniche che comportano ridotta eliminazione della CO2 con l’aria espirata ed accumulo nel sangue, dal momento che come indicato nell'equazione, l'aumento della CO2 sposta l'equazione verso sinistra, producendo più bicarbonato. Un aumento della concentrazione dei bicarbonati indica, quasi sempre, un’alcalosi metabolica.
La PCO2 è utile per determinare se l'apparato respiratorio stia rispondendo fisiologicamente ad un sovraccarico di acidi e stia riducendo la PCO2 per compensare l'acidosi; in vaso di disturbi misti è importante per decidere se il disturbo primitivo è, per esempio un’acidosi metabolica compensata con iperventilazione che causa un’alcalosi respiratoria secondaria. La riduzione della PCO2 è una caratteristica dell'alcalosi respiratoria.
Invece, se il problema primario è di tipo respiratorio, per esempio insufficienza respiratoria associata con BPCO, la ridotta eliminazione di CO2 causa un aumento della PCO2 e sposterà l'equazione verso sinistra producendo un’acidosi respiratoria. Altre possibilità sono che l'acidosi respiratoria si sviluppi a causa di farmaci, per esempio gli analgesici oppiacei, che possono deprimere il centro respiratorio riducendo la frequenza respiratoria con conseguente ipoventilazione e ritenzione della CO2. Un aumento della PCO2 è una caratteristica dell'acidosi respiratoria.(Hamilton et al. 2017)
DIAGNOSI
Ci sono quattro disturbi primari acido-base: acidosi metabolica, alcalosi metabolica, acidosi respiratoria e alcalosi respiratoria. Poiché il compenso renale ai disturbi respiratori richiede da tre a cinque giorni per essere completata, l’acidosi e l’alcalosi di origine respiratoria possono essere ulteriormente suddivisi in acute e croniche
Per una diagnosi definitiva dei disturbi dell’equilibrio acido base è indispensabile conoscere innanzitutto l’emogasanalisi arteriosa (EGA) che permette di conoscere i valori di pH e PCO2.
Per una diagnosi accurata di un disturbo acido-base è c necessario onoscere anche la concentrazione degli elettroliti e dell’anione bicarbonato nel siero. La concentrazione del potassio (suoi aumenti o riduzioni si osservano in molti disturbi metabolici dell’equilibrio acido-base), e quella del sodio e dei cloruri, oltre a segnalare possibili iponatremia o ipernatremia , servono anche per il calcolo del gap anionico nel siero. Inoltre, nei pazienti con grave acidosi metabolica, può essere utile calcolare l’ampiezza della differenza rispetto al normale del gap anionico (delta anionico), del gap dei bicarbonati (delta dei bicarbonati) e il rapporto fra i due delta (rapporto delta/delta).
Il sangue venoso periferico può essere raramente usato al posto dell’EGA, come procedura meno invasiva e meno costosa rispetto al prelievo arterioso. Tuttavia, questa pratica è gravata da numerosi limiti e può condurre ad errori, per cui si preferisce il sangue arterioso.
Quando si interpreta un’EGA, è utile ricordare che un pH normale non esclude l’esistenza di un disordine del metabolismo acido-base e seguire un metodo che può essere questo suggerito in 5 fasi o atti.
Atto 1 - Guardare il pH
Il pH può essere normale, aumentato (alkaliemia, pH>7,45) o diminuito (pH<7,35). Se il pH aumenta gli idrogenioni sono diminuiti, se il pH diminuisce è perché gli ioni H+ sono aumentati.
Atto 2 – Guardare i bicarbonati
La riduzione della concentrazione dei bicarbonati (limite inferiore 21-22mEq/L e limite superiore 27-29 mEqL nella maggior parte dei laboratori) è la caratteristica distintiva dell'acidosi metabolica. Una ridotta concentrazione di bicarbonato significa generalmente che il più importante dei sistemi tampone dell'organismo viene utilizzato per neutralizzare l'eccesso di acido (idrogenioni) che si produce, per esempio, nella chetoacidosi o nell'acidosi lattica [8]. Un'altra spiegazione può essere che la concentrazione dei bicarbonati è ridotta a causa di perdite attraverso il tratto gastrointestinale (diarrea) o nei pazienti con malattie renali, nei quali possono essere ridotti sia la sintesi di nuovi bicarbonati che il riassorbimento tubulare di quelli filtrati con conseguente perdita nelle urine. La riduzione della concentrazione dei bicarbonati è la caratteristica distintiva dell'acidosi metabolica [8].
Un aumento della concentrazione dei bicarbonati indica che vi sono state perdite significative di acidi dai fluidi corporei, per esempio in seguito a prolungata aspirazione nasogastrica o per vomito persistente [6]. L'aumento dei bicarbonati può esprimere anche il compenso cronico da parte dei reni in soggetti con ipoventilazione da malattie respiratorie croniche che comportano ridotta eliminazione della CO2 con l’aria espirata ed accumulo nel sangue, dal momento che come indicato nell'equazione, l'aumento della CO2 sposta l'equazione verso sinistra, producendo più bicarbonato. Un aumento della concentrazione dei bicarbonati indica, quasi sempre, un’alcalosi metabolica.
La risposta compensatoria deve essere valutata anche in base alla storia del paziente, soprattutto nel disturbi dell’equilibrio acido-base di origine respiratoria, dal momento che la risposta compensatoria renale è lenta. Pertanto, il livello previsto di compensazione è minore nei pazienti con disturbi respiratori acuti rispetto alle malattie respiratorie croniche. Come abbiamo già detto, la normale risposta compensatoria all'acidosi respiratoria prevede un aumento della concentrazione di HCO3 del siero di circa 1 mEq/L per ogni 10 mmHg di aumento della PCO2 in fase acuta e di circa 3,5- 5 mEq / L per ogni 10 mmHg di aumento della PCO2 se il problema respiratorio sottostante persiste per più di 3-5 giorni.
Atto 3 – Valutare la pCO2
La pCO2 è utile per determinare se l'apparato respiratorio sta rispondendo fisiologicamente ad un sovraccarico di acidi e stia riducendo la PCO2 per compensare l'acidosi; in caso di disturbi misti è importante per decidere se il disturbo primitivo è, per esempio un’acidosi metabolica compensata con iperventilazione che causa un’alcalosi respiratoria secondaria [8].
La riduzione della PCO2 è una caratteristica dell'alcalosi respiratoria. Invece, se il problema primario è di tipo respiratorio, per esempio insufficienza respiratoria associata con BPCO, la ridotta eliminazione di CO2 causa un aumento della PCO2 e sposterà l'equazione verso sinistra producendo un’acidosi respiratoria [6]. Altre possibilità sono che l'acidosi respiratoria si sviluppi a causa di farmaci, per esempio gli analgesici oppiacei, che possono deprimere il centro respiratorio riducendo la frequenza respiratoria con conseguente ipoventilazione e ritenzione della CO2[9,9]. Un aumento della PCO2 è una caratteristica dell'acidosi respiratoria.
Atto 4 – Diagnosi del disturbo dell’equilibrio acido base. Semplice o misto?
L'acidosi respiratoria è caratterizzata da riduzione del pH arterioso con aumento dei bicarbonati e della PCO2. Il sospetto origina da una Pco2> 40 mmHg; mentre l'HCO3− deve compensare in fase acuta aumentando di 3-4 mEq/L (3-4 mmol/L) per ogni aumento di 10 mmHg di Pco2 che perduri per almeno 4-12 h (ma può non esserci un incremento o esserci un incremento di soli 1-2 mEq/L. Un aumento maggiore dell'HCO3− suggerisce un'alcalosi metabolica primaria; un incremento minore suggerisce che non vi sia stato tempo per il compenso o che coesista un'acidosi metabolica primaria.
L'alcalosi respiratoria è caratterizzata da riduzione dei bicarbonati e della PCO2 e da pH aumentato. Nell'alcalosi respiratoria tipicamente la Pco2 è < 38 mmHg. e l'HCO3− compensa in 4-12 h riducendo la sua concentrazione di 4-5 mEq/L (4-5 mmol/L) per ogni 10 mmHg di riduzione della Pco2. Una riduzione di minore indica che non c'è stato tempo per la compensazione o che coesiste un'alcalosi metabolica primaria. Un decremento maggiore indica la presenza di un'acidosi metabolica primaria.
L'alcalosi metabolica è caratterizzata da aumento del pH arterioso, della pCO2 e dei bicarbonati. L'alcalosi metabolica presenta in genere HCO3−> 28 mEq/L (> 28 mmol/L). La Pco2 compensa aumentando di circa 0,6-0,75 mmHg per ogni 1 mEq/L (1 mmol/L) di aumento dell'HCO3− (fino a circa 55 mmHg). Un aumento maggiore indica un'acidosi respiratoria concomitante; un incremento minore, la coesistenza di un'alcalosi respiratoria.
L'acidosi metabolica è caratterizzata da riduzione del del pH arterioso, dei bicarbonati e della PCO2. Il compenso prevede una riduzione di circa 1,2 mmHg della Pco2 per ogni 1 mmol/L di diminuzione dell'HCO3−; il gap anionico. può essere normale o aumentato. Tipicamente i livelli sierici di HCO3− < 24 mEq/L (< 24 mmol/L).
Disturbi misti
Alcuni pazienti hanno due, tre, o più disturbi acido-base relativamente indipendenti. Questi disturbi misti includono combinazioni di disturbi metabolici (ad esempio, alcalosi metabolica indotta dal vomito, oltre all'acidosi lattica indotta da ipovolemia), disturbi metabolici e respiratori misti (ad esempio, acidosi metabolica e alcalosi respiratoria nell'intossicazione salicilica) e combinazioni più complesse. Come discusso nella sezione precedente, la valutazione dei pazienti con disturbi del metabolismo acido-base richiede inizialmente l'identificazione del disturbo maggiore e poi la valutazione se il grado di compenso sia o meno appropriato. Se la risposta compensatoria non è appropriata, allora è necessario sospettare un secondo disturbo sovrapposto e di trovarsi di fronte a un disturbo misto acido-base. Una compensazione significativamente ridotta o aumentata rispetto all’atteso è indicativa di un disturbo acido-base misto. Con l'eccezione dell'alcalosi respiratoria cronica e dell'acidosi respiratoria lieve- moderata, le risposte compensatorie, di solito, non riescono a riportare il pH arterioso completamente all’interno dei valori normali. Pertanto, un normale pH arterioso in presenza di variazioni significative sostanziali sia dell’HCO3 nel siero che della PCO2 arteriosa suggerisce l’esistenza di un disturbo misto (per esempio un'alcalosi respiratoria acuta iatrogenica se il fastidio e il dolore causati dal prelievo arterioso spingono il paziente a iperventilare. Se l'acidosi metabolica è il disturbo primario, una PCO2 arteriosa significativamente superiore alla risposta compensatoria prevista indica disturbo misto con acidosi metabolica e acidosi respiratoria, mentre una PCO2 arteriosa sostanzialmente inferiore al previsto definisce un disturbo misto di acidosi metabolica e alcalosi respiratoria, che potrebbe essere prodotta dall'iperventilazione acuta stimolata dal disagio del prelievo arterioso.
Se l'acidosi respiratoria è il disturbo principale, l’HCO3 nel siero deve essere adeguatamente aumentato. Se l’HCO3 nel siero non è aumentato secondo le previsioni, probabilmente coesiste anche un'acidosi metabolica e il pH arterioso può essere significativamente ridotto. Invece, se il HCO3 nel siero è più alto del previsto, l'alcalosi metabolica complica l'acidosi respiratoria e il pH arterioso può esser inappropriatamente "normale".
Determinare se il gap anionico è aumentato o normale, soprattutto nei pazienti con acidosi metabolica. Se il divario anionico aumenta, è utile valutare il rapporto tra l'aumento del gap anionico e la diminuzione della concentrazione di HCO3. Questo è chiamato il rapporto fra i due delta o rapporto delta/delta, cioè delta anion gap/delta HCO3 .
Nei pazienti con acidosi metabolica e gap anionico aumentato, le diagnosi di acidosi metabolica mista e alcalosi metabolica sono possibili in base al calcolo e all’interpretazione del rapporto delta/delta .
Atto 5 – Identificazione della causa che ha determinato lo squilibrio del metabolismo acido- base e altri altri test diagnostici . Una volta identificato il disturbo acido-base, o i disturbi misti, è necessario identificare la causa o le cause sottostanti di ogni disturbo e decidere il trattamento più appropriato. Molte volte la diagnosi eziologica è già evidente in base alla storia clinica e all’esame obiettivo del paziente, per cui questa fase può in effetti diventare la prima dell’intero percorso diagnostico.
Tabella 1 - Cause e meccanismi dei principali squilibri del metabolismo acido-base
|
|
Laboratorio |
Meccanismo principale |
Esempi |
|
Acidosi metabolica |
pH=D; bicarbonati =D; pCO2=D |
Riduzione dei bicarbonati |
Eccessiva formazione di idrogenioni (acidosi lattica, chetoacidosi Ridotta escrezione di idrogenioni (insufficienza renale) Eccessiva perdita di bicarbonati (diarrea) |
|
Alcalosi metabolica |
pH=A; bicarbonati =A; pCO2=A |
Aumento dei bicarbonati |
riduzione del volume extracellulare (vomito, diuretici) eccessiva perdita di potassio con iperaldosteronismo |
|
Acidosi respiratoria |
pH=D; pCO2=A; bicarbonati =A |
aumento della PaCO2 |
Riduzione della ventilazione efficace (BPCO, altre malattie respiratorie croniche); depressione farmacologica del centro del respiro |
|
Alcalosi respiratoria |
pH=A; pCO2=D; bicarbonati =D |
Riduzione della PaCO2 |
Aumentata ventilazione (ipossia, compenso dell’acidosi metabolica) |
Riferimenti bibliografici
- Malatesha G, Singh NK, Bharija A, Rehani B, Goel A. Comparison of arterial and venous pH, bicarbonate, PCO2 and PO2 in initial emergency department assessment. Emerg Med J EMJ. 2007; 24: 569–71.
- Chu Y-C, Chen C-Z, Lee C-H, Chen C-W, Chang H-Y, Hsiue T-R. Prediction of arterial blood gas values from venous blood gas values in patients with acute respiratory failure receiving mechanical ventilation. J Formos Med Assoc Taiwan Yi Zhi. 2003; 102: 539–43.
- Kelly A-M, Kyle E, McAlpine R. Venous pCO(2) and pH can be used to screen for significant hypercarbia in emergency patients with acute respiratory disease. J Emerg Med. 2002; 22: 15–9.
- Walkey AJ, Farber HW, O’Donnell C, Cabral H, Eagan JS, Philippides GJ. The accuracy of the central venous blood gas for acid-base monitoring. J Intensive Care Med. 2010; 25: 104–10.
- Malinoski DJ, Todd SR, Slone S, Mullins RJ, Schreiber MA. Correlation of central venous and arterial blood gas measurements in mechanically ventilated trauma patients. Arch Surg Chic Ill 1960. 2005; 140: 1122–5.
- DuBose Jr Thomas D. Acidosis and Alkalosis. In: Jameson JL, Fauci AS, Kasper DL, Hauser SL, Longo DL, Loscalzo J, editors. Harrison’s Principles of Internal Medicine, 20e [Internet]. New York, NY: McGraw-Hill Education; 2018 [cited 2020 Apr 2]. Available from: accessmedicine.mhmedical.com/content.aspx?aid=1165777984
- Seifter JL, Chang H-Y. Disorders of Acid-Base Balance: New Perspectives. Kidney Dis [Internet]. 2017 [cited 2020 Mar 30]; 2: 170–86. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5260542/
- Hamilton PK, Morgan NA, Connolly GM, Maxwell AP. Understanding Acid-Base Disorders. Ulster Med J [Internet]. 2017 [cited 2020 Mar 30]; 86: 161–6. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5849971/
- Kraut JA, Madias NE. Metabolic acidosis: pathophysiology, diagnosis and management. Nat Rev Nephrol. 2010; 6: 274–85.
